Em 5 de julho, a Novo Nordisk lançou um ensaio clínico de fase III da injeção de CagriSema na China, cujo objetivo é comparar a segurança e eficácia da injeção de CagriSema com semeglutida em pacientes obesos e com sobrepeso na China.
A injeção de CagriSema é uma terapia combinada de ação prolongada em desenvolvimento pela Novo Nordisk, os principais componentes são o agonista do receptor GLP-1 (peptídeo-1 semelhante ao glucagon) e um cagrilintida análogo da amilina de ação prolongada.A injeção de CagriSema pode ser administrada por via subcutânea uma vez por semana.
O objetivo principal foi comparar CagriSema (2,4 mg/2,4 mg) com semeglutido ou placebo uma vez por semana por via subcutânea.A Novo Nordisk anunciou os resultados de um ensaio do CagriSema para o tratamento do diabetes estágio 2, que provou que o efeito hipoglicêmico do CagriSema é melhor que o do semeglutido, e quase 90% dos indivíduos atingiram a meta de HbA1c.
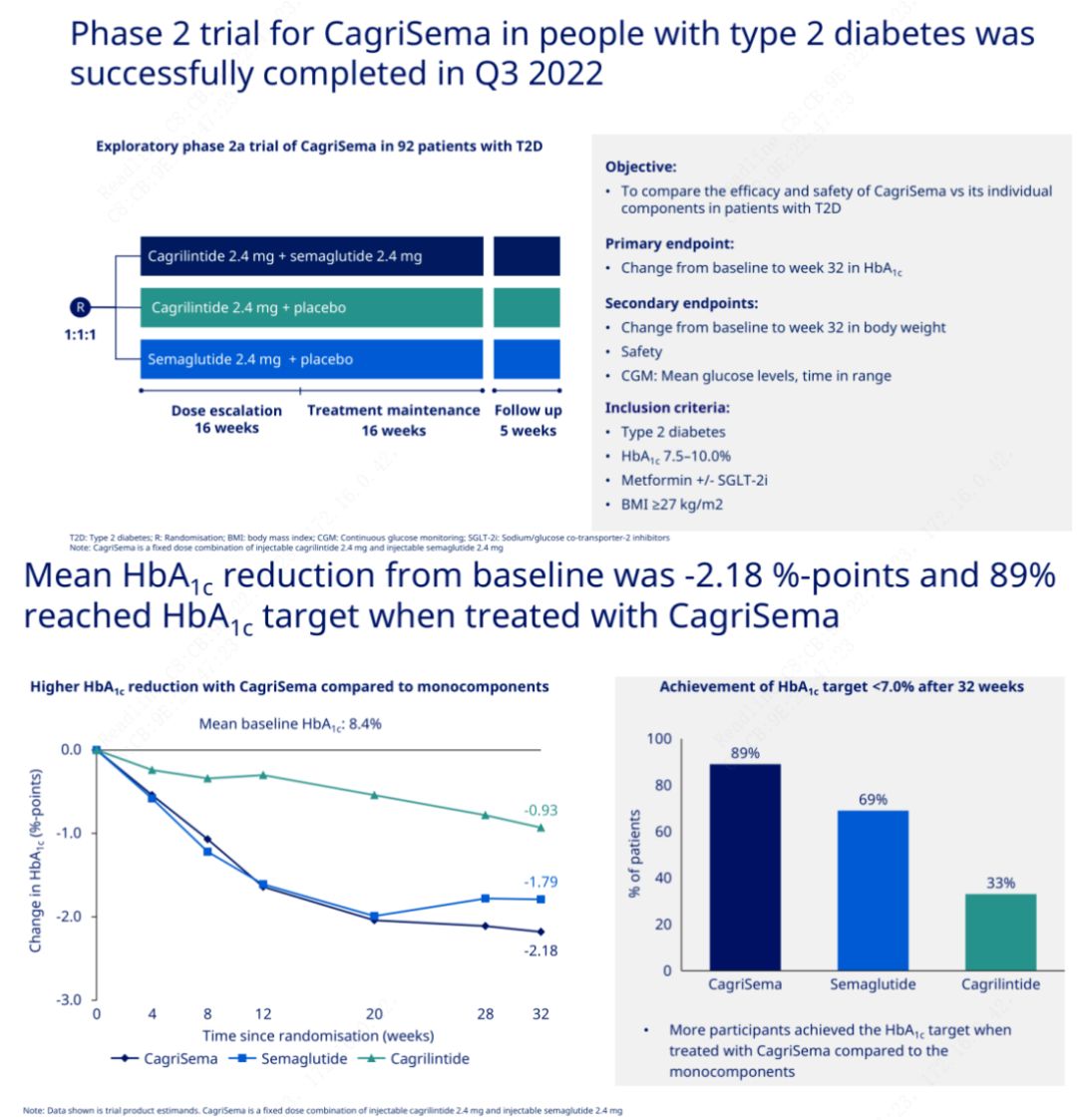
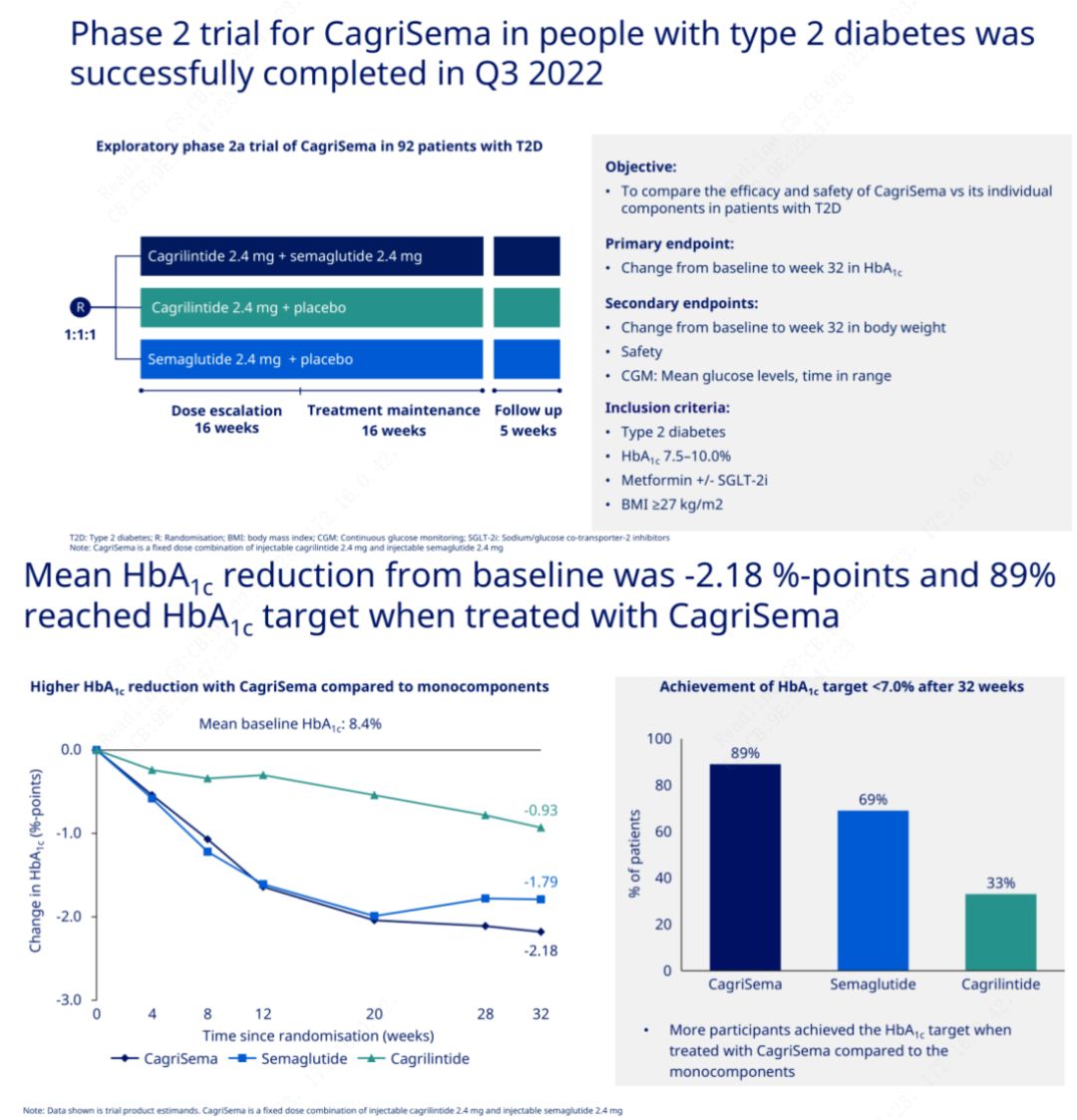
Os dados mostraram que, além do efeito hipoglicemiante significativo, em termos de perda de peso, a injeção de CagriSema superou significativamente o semeglutido (5,1%) e o cagrilintido (8,1%) com uma perda de peso de 15,6%.
O medicamento inovador Tirzepatide é o primeiro agonista semanal do receptor GIP/GLP-1 aprovado no mundo.Combina os efeitos de duas incretinas numa única molécula que é injetada uma vez por semana e é uma nova classe de tratamentos para a diabetes tipo 2.A tirzepatida foi aprovada pela Food and Drug Administration (FDA) dos EUA em maio de 2022 para melhorar o controle glicêmico (com base na dieta e exercícios) em adultos com diabetes tipo 2 e está atualmente aprovada na União Europeia, no Japão e em outros países.
Em 5 de julho, a Eli Lilly anunciou um estudo de fase III SURPASS-CN-MONO sobre a plataforma de registro de ensaios clínicos de medicamentos e divulgação de informações para o tratamento de pacientes com diabetes tipo 2.SURPASS-CN-MONO é um estudo de fase III randomizado, duplo-cego, controlado por placebo, projetado para avaliar a eficácia e segurança da monoterapia com tirzepatida em comparação com placebo em pessoas com diabetes tipo 2.O estudo planejou incluir 200 pacientes com diabetes tipo 2 que não estavam em uso de nenhum medicamento antidiabético nos 90 dias anteriores à Visita 1 (exceto em certas situações clínicas, como doença aguda, hospitalização ou cirurgia eletiva, de curto prazo (≤14 dias) uso de insulina).
Espera-se que diabetes tipo 2 seja aprovado este ano
No mês passado, os resultados de um estudo SURPASS-AP-Combo foram publicados em 25 de maio na revista de sucesso Nature Medicine.Os resultados mostraram que, em comparação com a insulina glargina, a Tirzepatida apresentou melhor HbA1c e redução de peso na população de pacientes com diabetes tipo 2 na região Ásia-Pacífico (principalmente China): redução de HbA1c de até 2,49% e redução de peso de até 7,2 kg (9,4%) às 40 semanas de tratamento, a melhoria significativa dos lípidos no sangue e da pressão arterial, e a segurança e tolerabilidade globais foram boas.
O ensaio clínico de Fase 3 do SURPASS-AP-Combo é o primeiro estudo da Tirzepatida conduzido principalmente em pacientes chineses com diabetes tipo 2, liderado pelo professor Ji Linong do Hospital Popular da Universidade de Pequim.SURPASS-AP-Combo é consistente com os resultados da série global de pesquisas SURPASS, o que prova ainda que a fisiopatologia do diabetes em pacientes chineses é consistente com a dos pacientes globais, o que é a base para a pesquisa e desenvolvimento simultâneo de novos medicamentos na China e no mundo, e também fornece evidências sólidas para dar aos pacientes chineses a oportunidade de usar os mais recentes medicamentos para tratamento do diabetes e sua aplicação clínica na China o mais rápido possível.
Horário da postagem: 18 de setembro de 2023

